近日,新加坡国立大学刘斌教授课题组成功开发了一种基于生物正交原理的可快速精准辨别和杀伤革兰氏阴性细菌、革兰氏阳性细菌的功能探针TPEPA(见图1C)。
首先,通过生物代谢工程的方法可分别使得阴性菌表面的脂多糖层和阳性菌肽聚糖层富含叠氮基官能团。TPEPA是一种具有聚集诱导发光特性的光敏剂。其具有良好的水溶性,在水溶液环境中的荧光极其微弱,同时TPEPA具有可与叠氮基团进行click反应的炔基,当炔基与阴性菌(阳性菌)表面的叠氮发生click反应后,TPEPA分子内运动被抑制使得荧光被“点亮”。根据革兰氏阴阳性菌细胞结构的不同,作者采用Kdo-N3糖和Ala-N3氨基酸分别对革兰氏阳性菌和阴性菌进行生物代谢处理后,可以实现TPEPA对革兰氏阳性菌和阴性菌的选择性检测与原位杀伤。
细菌感染引起的疾病正在以不可预测的速度快速增加,对人类的生命健康造成重大威胁。目前临床抗菌治疗的主要障碍是无法对多重细菌交叉感染进行快速、准确地诊断,进而错过最佳的治疗阶段。当前鉴别细菌病原体的诊断方法主要包括血液培养、组织样本、聚合酶链式反应(PCR)等。但是,这些方法存在检测时间长、精准度低、检测流程复杂以及需要依赖精密仪器等缺点。由于无法及时可靠地获取细菌病原体的信息,大多数细菌感染都根据医生的经验诊断并采用广谱抗生素予以治疗。广谱抗生素的普遍使用往往容易导致细菌产生耐药性。据估计,除非新的抗菌药物研究有重大进展,否则到2050年细菌感染致死将是导致人类死亡的主要原因。因此,设计并探讨可快速有效辨别和精确杀伤细菌病原体的方法具有重要意义。
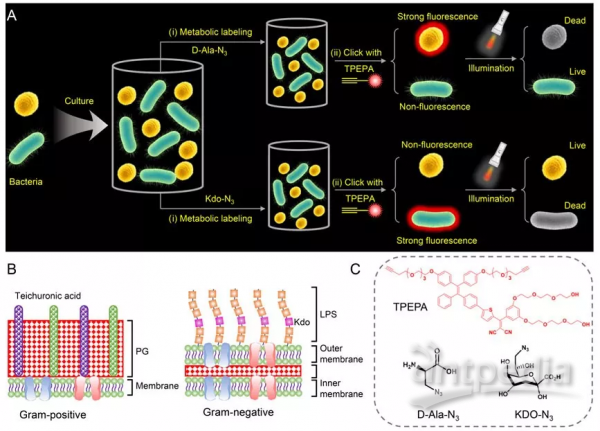
图1.TPEPA鉴别并杀伤革兰氏阴性菌和阳性菌的机理示意图
首先作者选用Escherichia coli(E.coli)作为革兰氏阴性菌的模型菌,在经过Kdo-N3代谢处理后,分别与不同浓度的TPEPA进行孵育(图1A),流式细胞计数结果显示E.coli的荧光强度具有浓度依赖性。临床上使用的菌落培养法检测细菌常常需要数天的时间,而TPEPA标记细菌的时间非常迅速。流式结果显示只需要半小时,大部分的E.coli细菌即可以被标记上近红外荧光(图2A)。接着作者选用Staphylococcus aureus(S.aureus)作为革兰氏阳性菌的代表菌,在经过D-Ala-N3代谢处理后,S.aureus也可被快速标记上近红外荧光。从激光共聚焦图中可以看到,TPEPA的红色荧光信号主要集中在E.coli和S.aureus细菌的外围(图2C3和2D4),而在细菌的细胞质中并没有发现红色荧光信号。其他革兰氏阳性菌(MRSA、Bacillus subtilis)和阴性菌(Salmonella typhimurium、Pseudomonas aeruginosa)中也发现类似的现象。
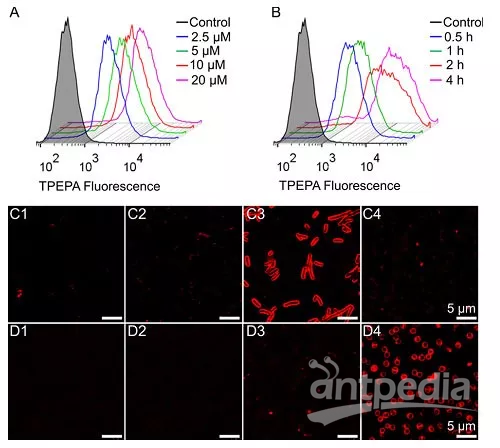
图2.功能探针TPEPA单独标记E.coli和S.aureus细菌能力的研究
接下来,作者考察了TPEPA选择性标记混合菌中革兰氏阴性菌和阳性菌的能力。首先作者将革兰氏阴性菌(E.coli)和革兰氏阳性菌(S.aureus)等比例混合得到混合细菌溶液。Kdo是革兰氏阴性菌LPS的重要组成成分,而革兰氏阳性菌中并没有LPS,因此经过Kdo-N3代谢处理后的革兰氏阴性菌可以被TPEPA选择性地标记,而革兰氏阳性菌并不能被标记。D-Ala可以代谢至革兰氏阴性菌和阳性菌的肽聚糖上。但是不同于革兰氏阳性菌,革兰氏阴性菌最外层有一层外膜,该外膜可以阻止分子量大于650 Da的分子进入细菌外膜。功能探针TPEPA分子量为1235 Da,因此在经过D-Ala-N3代谢处理后,混合菌中的革兰氏阳性菌可以被选择性被标记上(图3)。通过这样的策略,TPEPA可以快速精准地实现对革兰氏阴、阳性菌的鉴别。
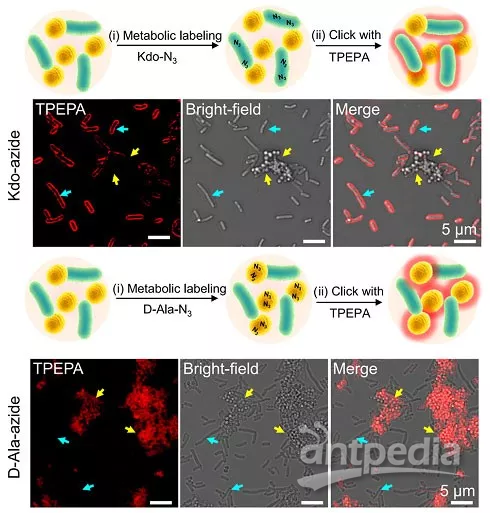
图3.功能探针TPEPA选择性标记混合细菌中E.coli或S.aureus的研究
TPEPA是一种具有聚集诱导发光特性的光敏剂,在光照下可以产生活性单线态氧进而有效地杀灭细菌。作者接下来研究了TPEPA对细菌的光照杀菌能力。细菌生存实验和扫描电镜实验结果都证明了TPEPA可以对革兰氏阴性菌和革兰氏阳性菌具有非常良好的光照杀菌能力(图4)。
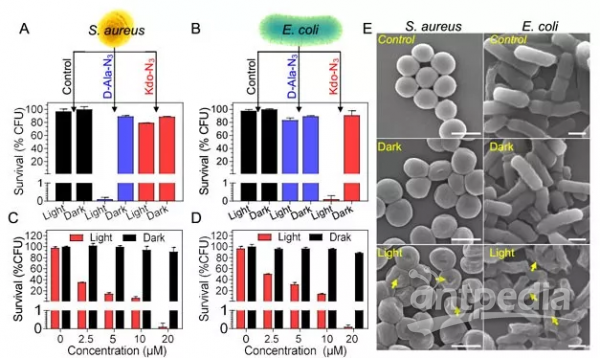
图4.功能探针TPEPA对E.coli和S.aureus的光照杀菌研究
总之,作者设计了一种生物相容性高且对革兰氏阴、阳性菌具有快速选择性成像和精确杀伤功能的探针,该探针在细菌诊断和细菌感染治疗等方面显示出巨大的应用前景。
该项目得到新加坡国家研究基金(R279-000-483-281、R279-000-444-281)和新加坡国立大学研究基金(R279-000-482-133)的资助。
课题组介绍
近年来,新加坡国立大学刘斌教授课题组主要研究和探索先进功能材料在生物医学和清洁能源等领域中的应用。在生物医学方面,致力于使用具有良好生物相容性的有机材料以实现对重要生物过程的高效便捷的示踪以及对一些疾病非侵入性的治疗;在清洁能源方面,主要设计合成高效的敏化剂和催化剂,用来将太阳能转化成简便易用的清洁能源。其成果多次发表在国际一流期刊。
通讯作者简介
刘斌,新加坡国立大学教授,化学与生物分子工程学院系主任,新加坡工程院院士,亚太材料科学院院士,英国皇家化学会会士。同时也是ACS Materials Letters执行主编,Advanced Materials、Advanced Functional Materials等多个杂志的编委。致力于共轭聚合物发光材料、聚集诱导发光材料等在生物医学及能源中的应用研究,其成果多次发表在国际一流期刊,h-因子89,连续多年荣获科睿唯安“高被引科学家”称号。其多项研究成果实现产业化并创立了LuminiCell公司。