
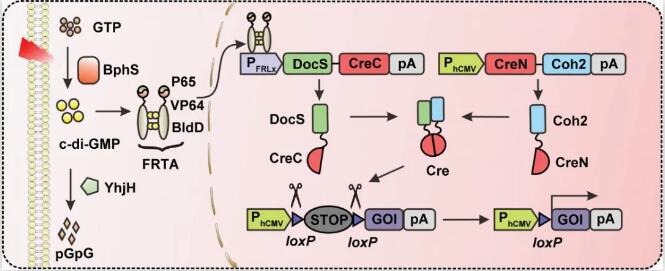
图1 FISC工作原理。在远红光照射下,细胞中的BphS利用GTP合成环二鸟苷酸c-di-GMP,c-di-GMP与转录激活结构BldD-P65-VP64 结合并进入细胞核,激活DocS-CreC60的表达;CreN59- Coh2在细胞中组成型表达。两部分Cre在DocS与Coh2蛋白相互作用下重新合成完整Cre重组酶,识别报告基因中loxP位点切除STOP序列,起始下游目的基因表达。
首先,研究团队人员通过优化不同启动子,不同质粒量,蛋白间连接肽以及不同Cre重组酶作用序列,得到了最优版本的FISC系统,最佳诱导基因表达倍数高达约120倍。另外,在哺乳细胞中测试了FISC系统动力学表征,结果显示在不同的报告蛋白和不同的细胞系中,FISC系统都展现出良好的调控效果。在HEK-293细胞中,FISC系统具有光照强度和时间依赖性以及高度的时空特异性。随后,研究团队人员通过流体动力学注射法将FISC系统递送到BALB/c小鼠体内,探究FISC系统在体内的工作情况,并与目前已发表的两套蓝光调控Cre-loxP系统进行比较,结果显示FISC系统在体内展现出更高效的基因重组效率(54.4倍),这也充分体现了远红光的组织穿透性优势,进一步证明了FISC系统在动物体内极具应用优势。
同时,研究团队人员采用电转的方法将FISC系统递送到tdTomato转基因报告小鼠肌肉中(Gt(ROSA)26Sortm14(CAG-tdTomato)Hze),小鼠经远红光照射后,在体内诱导合成的Cre重组酶会切割基因组上的loxP序列,切除STOP序列,表达tdTomato红色荧光蛋白。结果发现在mRNA和蛋白水平上FISC系统均展现出比蓝光调控的Cre-loxP系统更高的DNA重组效率。
腺相关病毒AAV因为其具有免疫原性低和非整合性等优势,目前是临床治疗上应用较为广泛的基因载体。为了实现体内高效递送,研究团队人员将FISC系统构建在AAV载体上,利用AAV病毒将FISC系统递送到tdTomato转基因报告小鼠中。通过观察小鼠活体成像和肝脏成像,与黑暗组小鼠相比,光照组小鼠红色荧光蛋白表达量显著升高。这说明利用AAV载体成功实现了FISC系统在小鼠体内介导的DNA重组。
总之,FISC系统在体内外实现了精准可控的基因改造,并具有深度组织渗透能力和低毒性。这项研究将有望为细胞的命运图谱的研究、功能基因的研究以及动物模型的构建等提供一种新的策略和方法。
据悉,叶海峰研究员为该论文的通讯作者,2017级博士研究生吴嘉丽、王美艳副研究员和2018届硕士研究生杨雪平为该研究论文的共同第一作者。
研究背景
本研究是叶海峰课题组在光遗传学应用上的进一步的研究成果。
2017年,该课题组在Science Translational Medicine期刊上发表了一篇研究文章(【独家专访】华东师大叶海峰组首次通过智能手机实现远程调控治疗糖尿病),文章报道了一种远红光(730 nm,LED)调控的转基因表达控制系统,并实现了智能手机远程控制光敏细胞释放胰岛素治疗糖尿病的目标。
2018年,该课题组在PNAS上发表研究论文(亮点推荐丨叶海峰组实现远红光控制细胞命运),将远红光调控转基因表达控制系统与CRISPR-dCas9技术相结合,开发了远红光调控的CRISPR-dCas9内源基因转录激活装置(FACE),可实现表观遗传操控以及诱导干细胞分化为功能性神经细胞。
2020年,该课题组在Science Advances 上发表研究论文(亮点推荐 | 叶海峰团队利用“光刀”实现基因时空特异性的精准编辑),将远红光调控转基因表达控制系统与CRISPR-Cas9技术相结合,开发了一个远红光调控的分割型split-Cas9基因编辑系统(FAST),通过对小鼠肿瘤中的致癌基因进行编辑,成果实现了光控抑制肿瘤生长。该一系列研究工作进一步拓展了光遗传学工具箱,为精准可控的细胞治疗和基因治疗奠定了研究基础,进一步推动了基于光遗传学的精准治疗和临床转化应用。
关于Cre-loxP重组酶系统
Cre-loxP重组酶系统是一种位点特异的基因重组技术,可以迅速而有效地实现各种生理环境下的基因定点插入、删除、替换和倒位等操作,具有高效性,特异性强,应用范围广等特点。近年来,科学家将合成生物学理念融入Cre-loxP重组酶系统中,开发出了一系列调控式的Cre-loxP重组酶系统,如化学方法诱导的Cre-loxP重组酶系统和紫光/蓝光诱导的Cre-loxP重组酶系统。但是这些诱导系统仍然具有一定程度的毒性,并且紫蓝光的组织穿透性差,这些都极大地限制了Cre-loxP重组酶系统在动物体内的应用。