
免疫学教授Michael Farzan博士与团队。图片来源:Scripps研究所
《Nature Biotechnology》报道了这一壮举,基因疗法通过将治疗性基因的拷贝插入患者的细胞来发挥作用,但是一旦将基因拷贝传递到患者的细胞中,就无法将其关闭或调节,因此迄今为止只有少数几种基因疗法被FDA批准。正是缺乏这样一种基本的安全特性限制了基因疗法的发展,这项技术解决了一个主要的安全问题,扩大了其使用范围。

研究人员从一个锤头状核酶的RNA分子家族中制备了转基因开关,这些核酶具有非凡的特性,一旦将其从编码的DNA转录到RNA中,便被切成两半。因此含有这种核酶的DNA的治疗性转基因的转录本往往是分成两部分的,然而,核酶的这种自我切割作用可以被锁在核酶活性位点上的RNA样吗啉代阻断,这时转基因转录本将保持完整并被翻译成治疗性蛋白质。核酶有效地充当了转基因的“关闭开关”,而注射到转基因所在组织中相匹配的吗啉代能有效地使转基因重新“打开”,其程度取决于吗啉代的剂量。科学家们从一种称为N107的锤头状核酶开始,经过几个月的实验修饰核酶,直到其动态范围扩大数十倍。
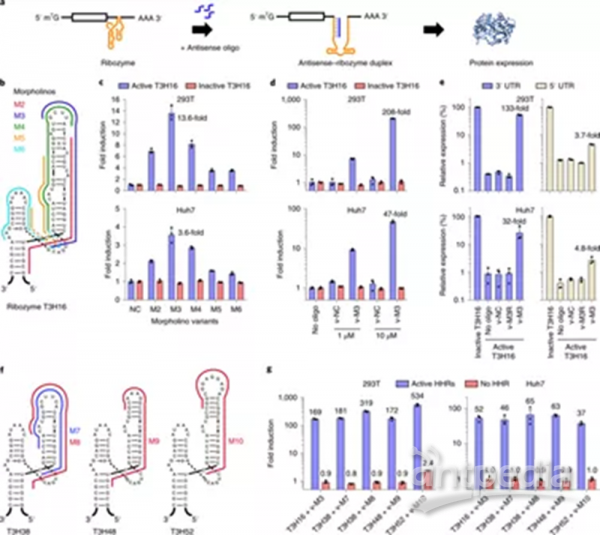
使用优化的III型核酶可有效调节基因表达
研究小组随后在EPO基因疗法的小鼠模型中展示了基于核酶的开关,该模型虽然尚未获得FDA批准,但被认为比目前用于治疗与严重肾脏疾病相关的贫血的方法更好。他们向小鼠的肌肉组织中注射了EPO转基因,结果表明嵌入的核酶将EPO的产生抑制到非常低的水平,然后将少量的吗啉代分子注射到受影响的组织中,极大地逆转了这种抑制作用,EPO的产量增加200倍以上并且持续了一周以上,而标准注射的EPO半衰期只有几个小时。这些特性使基于核酶的开关具有实际的临床应用潜能。
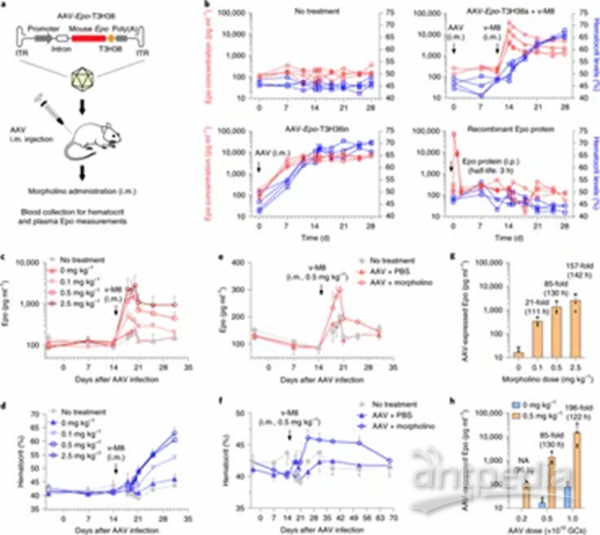
EPO转基因的体内调节
Farzan认为这种方法“是目前调节动物或人类基因疗法剂量的唯一实用方法”,该技术的简单性以及吗啉代已获得FDA批准的事实,可以使新的转基因开关系统用于各种设想的基因疗法中。在未来的研究中,Farzan和他的同事们将努力适应他们的核酶开关技术,以便将其用作基因疗法的故障保护机制,从而使错误的转基因永久性地失活。
参考资料:
[1] New technology allows control of genetherapy doses
[2] A reversible RNA on-switch thatcontrols gene expression of AAV-delivered therapeutics in vivo