试验过程中,生物样本可能是最敏感的,因为它们的活性和特性依赖于合适的试验操作和贮藏条件。实验室菌种的处理和保藏的程序应标准化,使尽可能减少菌种污染和生长特性的改变。按统一操作程序制备的菌株是微生物试验结果一致性的重要保证。(对于菌株的验收,复苏传代,使用,必须有规范化的程序,以保证菌株的标准特性)
微生物检验用的试验菌应来自认可的国内或国外菌种收藏机构的标准菌株,或使用与标准菌株所有相关特性等效的商业派生菌株。(一般是ATCC国内也有CMCC,食品相关的CICC的菌株也可以。)
标准菌株的复活或培养物的制备应按供应商提供的说明或按已验证的方法进行。从国内或国外菌种收藏机构获得的标准菌株经过复活并在适宜的培养基中生长后,即为标准储备菌株。标准储备菌株应进行纯度和特性确认。标准储备菌株保存时,可将培养物等份悬浮于抗冷冻的培养基中,并分装于小瓶中,建议采用低温冷冻干燥,液氮储存,超低温冷冻(低于-30℃)等方法保存。低于-70℃或低温冷冻干燥方法可以延长菌种保存时间。标准储备菌株可用于制备每月或每周一次转种的工作菌株。冷冻菌种一旦解冻转种制备工作菌株后,不得重新冷冻和再次使用。
工作菌株的传代次数应严格控制,不得超过 5 代(从菌种收藏机构获得的标准菌株为第 0 代),以防止过度的传代增加表型变化的风险。1代是指将活的培养物接种到微生物生长的新鲜培养基中培养,任何亚培养的形式均被认为是转种或传代一次。必要时,实验室应对工作菌株的特性和纯度进行确认。
工作菌株不可代替标准菌株,标准菌株的商业衍生物仅可用作工作菌株。
在这里有些概念需要理顺:
标准菌株,这里指的是冻干菌粉。
储备菌株:复苏后的1代培养物。
工作菌株:由储备菌株转种传代而来。
实验室必须建立和保存其所有菌种的进出、收集、贮藏、保存、确认试验以及销毁的记录(有了程序,就应该有配套的记录),应有文件化的程序管理菌种(从标准菌株到工作菌株),该程序包括:标准菌种的申购记录;从标准菌株到工作菌株操作及记录;菌种必须定期转种传代,并做纯度、特性等实验室所需关键诊断指标的确认,并记录;每支菌种都应适当标注,注明其名称、标准号、接种日期、所传代数;菌种生长的培养基和培养条件;菌种保存的位置和条件;其它需要的程序。
标准菌株复活
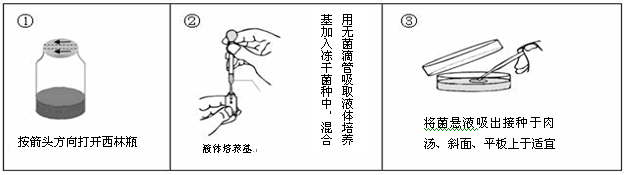
1、安瓿bai瓶装微生物菌种开封
1-1、用浸过70%酒精的du脱脂棉擦净安瓿瓶。
1-2、用火焰将安瓿瓶口加热灭菌。
1-3、用镊子将铝封口撕开。
2、菌株恢复培养
2-1、用无菌吸管,吸取0.3-0.4ml适宜的液体培养基,滴入安瓿管内,轻轻振荡,使冻干菌体溶解呈悬浮状。
2-2、取约0.2ml菌体悬浮液,移植于指定的琼脂斜面培养基上,剩余的菌液,注入指定的液体培养基内(3-4mL),然后在建议的温度下培养。
三、注意事项
3-1、菌种活化前,请将安瓿瓶保存在5-10℃的环境下。
3-2、厌氧菌的培养,如无特别说明,自开封至接种完成,均需以无氧气体充填,以保持厌氧状态。
3-3、某些菌种经过冷冻干燥保存后,延迟期较长,需连续两次继代培养才能正常生长。